光镊解开化疗药物对DNA的影响
康奈尔大学的新研究为一种常见的化疗药物依托泊苷如何阻止和毒害使癌细胞蓬勃发展的基本酶提供了新的视角。
来自James Gilbert White物理科学杰出教授和艺术与科学学院霍华德休斯医学研究所研究员Michelle Wang实验室的研究结果将推进一系列癌症抑制剂的研究。该小组开发的技术还将能够创建灵敏的筛查工具,以确定可以改善患者治疗的药物机制。
该小组的论文“依托泊苷通过拓扑异构酶II促进DNA环捕获和屏障形成”于30月<>日发表在Nature Chemical Biology上。共同主要作者是研究专家Tung Le和博士后研究员Meiling Wu。
40年来,依托泊苷一直是治疗多种癌症的值得信赖的化疗药物。依托泊苷通过靶向IIA型真核拓扑异构酶(也称为拓扑IIs)成功,这些酶使癌细胞能够复制。
复制过程的中心是长而纠缠的螺旋盘绕的DNA链。为了使癌症扩散,这些链需要被运动蛋白解开、旋转和复制。Topo II非常适合这项工作。
他们表演了一种精心设计的绳索技巧,通过切割来放松超螺旋的DNA,非常快速地将另一条DNA链穿过中间,然后将切割的DNA重新连接在一起。所有这些都是在不破坏DNA微妙的遗传结构的情况下完成的 - 这是一项令人难以置信的,令人难以置信的快速生物学壮举,每天在体内发生大约300亿次。
依托泊苷的伟大优点是它可以在任何东西重新连接之前稳定DNA双链断裂,从而防止癌细胞复制。然而,依托泊苷如何与DNA结构相互作用的复杂性仍然模糊不清。
“我们通常会问:研究DNA上发生的分子机器的最佳方法是什么?”“王祺说。“为了了解这些酶是如何工作的,我们想模仿细胞中可能发生的情况。运动蛋白拉动DNA或对DNA施加力。所以我们说,好吧,我们可以施加力量,看看会发生什么。
Wang的实验室使用三种不同的单分子操作技术来观察依托泊苷对三种拓扑II的影响,这些技术由约翰霍普金斯大学James Berger教授领导的合作者提供:酵母拓扑异构酶II,人拓扑异构酶II α和人拓扑异构酶II β。
“DNA拓扑,在概念上和扭转力学性能方面,人们真的很难掌握,”王说。“研究它的方法很少。但我们碰巧拥有合适的工具。我们拥有合适工具的原因是,在过去的20年里,我们一直在努力开发它们。这些工具和这个问题恰好在正确的时间融合在一起。
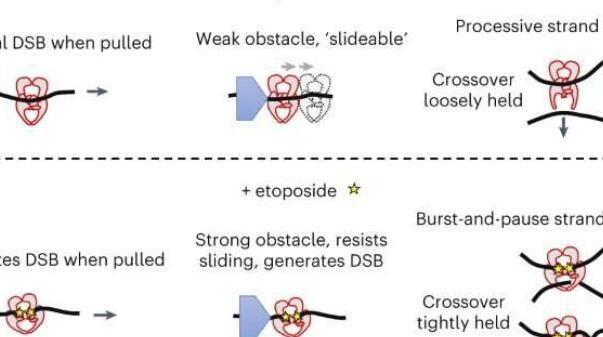
首先,研究人员使用光镊将DNA拉伸成各种配置,展示了依托泊苷如何压缩,释放和破坏它,并产生DNA环。这种环捕获行为让所有人感到惊讶,因为它揭示了依托泊苷的新影响,这是以前未知的。这意味着依托泊苷可以促进拓扑II显著改变体内DNA结构和拓扑结构。
他们的第三种技术是磁性镊子的版本,其中他们用结合的拓扑II扭曲DNA,并观察拓扑II以稳定的速率放松DNA。当他们添加依托泊苷时,他们发现化学物质错开了这种模式,引入了与超螺旋环捕获相关的停顿。
通过捕获依托泊苷增强这些作用并干扰拓扑II功能的不同方式,研究人员现在有一个定量系统来表征其他拓扑异构酶药物的行为。
“我认为这为我们提供了一套工具,使我们能够以非常全面的方式研究许多不同种类的拓扑异构酶和其他种类的药物,”王说。“我们所做的一切都模仿体内发生的事情。我们只是以机械控制的方式进行。这就是它如此强大的原因。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
【首都师范大学是211吗】一、“首都师范大学是211吗”是许多考生和家长在选择大学时经常提出的问题。实际上,...浏览全文>>
-
【首都师范大学科德学院自考和统招毕业证不一样吗有什么不一样的】在选择继续教育方式时,很多学生都会关注“...浏览全文>>
-
【首都师范大学科德学院自考本科国家承认学历吗】一、“首都师范大学科德学院自考本科国家承认学历吗”是许多...浏览全文>>
-
【首都师范大学科德学院怎么样首都师范大学科德学院介绍】首都师范大学科德学院是一所位于北京市的全日制本科...浏览全文>>
-
【第一次电影剧情】《第一次》是一部由美国导演理查德·林克莱特(Richard Linklater)执导的电影,于2004年...浏览全文>>
-
【首都师范大学科德学院学费一年多少钱】首都师范大学科德学院是一所经教育部批准设立的全日制本科独立学院,...浏览全文>>
-
【第一次点外卖的流程】对于第一次尝试点外卖的人来说,整个过程可能会有些陌生。不过,只要按照步骤来,就能...浏览全文>>
-
【首都师范大学科德学院学费为什么要这么贵】首都师范大学科德学院作为一所独立学院,近年来在学费方面引发了...浏览全文>>
-
【第一次登泰山的忌讳】泰山,作为五岳之首,不仅是中国文化的重要象征,也是无数人心中的朝圣之地。对于第一...浏览全文>>
-
【首都师范大学科德学院位于哪个城市】首都师范大学科德学院是一所独立学院,隶属于首都师范大学。对于许多学...浏览全文>>
