表观遗传信息的丢失会导致衰老 恢复可以逆转它
一项进行了 13 年的国际研究首次表明,DNA 组织和调节方式的退化(称为表观遗传学)可以驱动生物体衰老,而与遗传密码本身的变化无关。
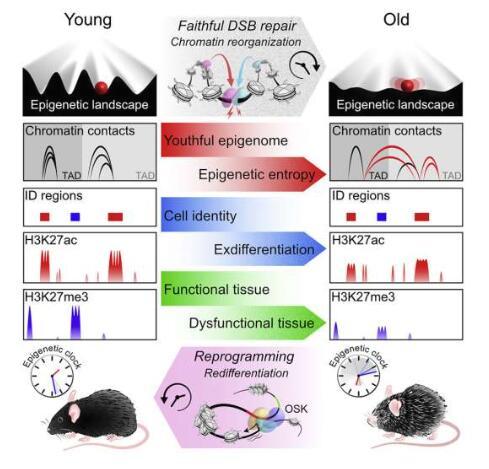
这项工作表明,表观遗传信息的崩溃会导致小鼠衰老,而恢复表观基因组的完整性会逆转这些衰老迹象。
调查结果于 1 月 12 日在线发布在Cell上。
“我们相信我们的研究是第一项表明表观遗传变化是哺乳动物衰老的主要驱动因素的研究,”该论文的资深作者、哈佛医学院布拉瓦尼克研究所遗传学教授、Paul F 研究所联合主任大卫辛克莱说。 . 格伦衰老研究生物学中心。
该团队广泛的系列实验提供了人们期待已久的确认,即 DNA 变化不是唯一——甚至不是主要的——衰老原因。相反,研究结果表明,染色质(形成染色体的 DNA 和蛋白质的复合物)的化学和结构变化会在不改变遗传密码本身的情况下加速衰老。
“我们预计这些发现将改变我们看待衰老过程的方式以及我们治疗与衰老相关疾病的方式,”共同第一作者、辛克莱实验室遗传学研究员 Jae-Hyun Yang 说。
作者说,由于操纵控制表观遗传过程的分子比逆转 DNA 突变更容易,因此这项工作指出了关注表观遗传学而非遗传学的新途径,以预防或治疗与年龄相关的损伤。
首先,这些结果需要在大型哺乳动物和人类身上得到复制。目前正在进行对非人类灵长类动物的研究。
“我们希望这些结果被视为我们控制衰老能力的转折点,”辛克莱说。“这是第一项表明我们可以精确控制复杂动物的生物学年龄的研究;我们可以随意驱动它前进和后退。”
超越突变
对于研究衰老的人来说,最紧迫的问题也许是衰老的原因。
几十年来,该领域的一个主流理论是,衰老是由 DNA 变化的积累引起的,主要是基因突变,随着时间的推移,这些变化会阻止越来越多的基因正常发挥作用。这些故障反过来又会导致细胞失去其身份,从而导致组织和器官崩溃,导致疾病并最终导致死亡。
然而,近年来,越来越多的研究表明,这个故事还有更多的意义。
例如,一些研究人员发现,一些具有高突变率的人和老鼠并没有表现出过早衰老的迹象。其他人观察到许多类型的老化细胞几乎没有或没有突变。
研究人员开始想知道还有什么可以与 DNA 变化一起或代替 DNA 变化来导致衰老。可能的罪魁祸首名单越来越长。其中包括表观遗传变化。
表观遗传学的一个组成部分是物理结构,例如将 DNA 捆绑成紧密压缩的染色质并在需要时展开该 DNA 部分的组蛋白。当基因被捆绑在一起时,它们是不可访问的,但当它们被解开时,可以被复制并用于生产蛋白质。因此,表观遗传因素调节在任何给定时间在任何给定细胞中哪些基因是活跃的或不活跃的。
通过充当基因活动的开关,这些表观遗传分子有助于定义细胞类型和功能。由于生物体中的每个细胞都具有基本相同的 DNA,因此正是特定基因的开关将神经细胞、肌肉细胞和肺细胞区分开来。
“表观遗传学就像一个细胞的操作系统,告诉它如何以不同的方式使用相同的遗传物质,”Yang 说,他是辛克莱实验室的前博士后研究员 Motoshi Hayano 的共同第一作者,现就职于庆应义塾大学东京医学。
在 1990 年代末和 2000 年代初,辛克莱的实验室和其他人在酵母和哺乳动物中表明,表观遗传变化伴随着衰老。然而,他们无法判断这些变化是导致衰老还是衰老的结果。
直到目前的研究,Sinclair 的团队才能够将表观遗传与遗传变化区分开来,并确认表观遗传信息的崩溃确实会导致小鼠衰老。
冰老鼠
该团队的主要实验涉及在实验室小鼠的 DNA 中创建临时的、快速愈合的切口。
这些断裂模仿了哺乳动物细胞每天对呼吸、暴露于阳光和宇宙射线以及接触某些化学物质等事物做出反应而经历的低级、持续的染色体断裂。
在这项研究中,为了测试这个过程是否会导致衰老,研究人员加快了休息的次数,以模拟快进的生活。
该团队还确保大部分断裂不会发生在小鼠 DNA 的编码区——构成基因的片段。这阻止了动物的基因发生突变。相反,断裂改变了 DNA 折叠的方式。
Sinclair 及其同事称他们的系统为 ICE,是表观基因组可诱导变化的缩写。
起初,表观遗传因素暂停了它们调节基因的正常工作,并转移到 DNA 断裂处以协调修复。之后,这些因素又回到了原来的位置。
但随着时间的推移,事情发生了变化。研究人员注意到,这些因素变得“分心”并且在修复休息后没有回家。表观基因组变得杂乱无章,并开始丢失其原始信息。染色质以错误的模式浓缩和脱线,这是表观遗传功能障碍的标志。
随着小鼠失去年轻的表观遗传功能,它们开始看起来和行为都变老了。研究人员发现表明衰老的生物标志物有所增加。细胞失去了它们的身份,例如肌肉或皮肤细胞。组织功能衰退。器官衰竭。
该团队使用辛克莱实验室最近开发的一种工具来测量老鼠的年龄,不是按时间顺序,按天或月计算,而是“生物学上”,基于基因组中有多少位点失去了通常附着在它们身上的甲基。与同时出生的未经治疗的小鼠相比,ICE 小鼠的年龄显着增加。
又年轻了
接下来,研究人员对小鼠进行了基因治疗,以逆转它们引起的表观遗传变化。
“这就像重新启动有故障的电脑,”辛克莱说。
该疗法传递了三个基因——Oct4、Sox2 和 Klf4,它们一起命名为 OSK——它们在干细胞中很活跃,可以帮助成熟细胞恢复到更早的状态。(Sinclair 的实验室在 2020 年使用这种鸡尾酒使失明老鼠恢复了视力。)
ICE小鼠的器官和组织恢复了年轻状态。
Sinclair 说,该疗法“启动了一个表观遗传程序,导致细胞恢复它们年轻时的表观遗传信息。” “这是永久重置。”
OSK 治疗究竟如何实现这一点尚不清楚。
Sinclair 说,在这个阶段,这一发现支持了这样的假设,即哺乳动物细胞维护着一种表观遗传软件的备份副本,当被访问时,可以让老化的、表观遗传混乱的细胞重新启动,进入年轻、健康的状态。
目前,广泛的实验使团队得出结论,“通过操纵表观基因组,可以向前和向后推动衰老,”杨说。
从这里
ICE 方法为研究人员提供了一种探索表观遗传学在衰老和其他生物过程中的作用的新方法。
由于 ICE 小鼠仅在六个月后就出现了衰老迹象,而不是在小鼠平均寿命两年半即将结束时出现,因此该方法还为研究衰老的研究人员节省了时间和金钱。
研究人员还可以超越 OSK 基因疗法,探索如何在衰老的生物体中恢复 丢失的表观遗传信息。
杨说:“还有其他方法可以操纵表观基因组,例如药物和诱导温和压力的小分子化学物质。” “这项工作为应用其他方法使细胞和组织恢复活力打开了一扇门。”
辛克莱希望这项工作能激励其他科学家研究如何控制衰老,以预防和消除人类与年龄相关的疾病和病症,例如心血管疾病、2 型糖尿病、神经退化和虚弱。
“这些都是衰老的表现,我们一直试图在它们出现时用药物治疗,这几乎为时已晚,”他说。
目标是解决衰老的根本原因,以延长人类的健康寿命:一个人不仅可以活着,而且可以保持健康的年数。
医学应用还有很长的路要走,需要在多种细胞和动物模型中进行广泛的实验。但是,辛克莱说,科学家们应该放眼长远,不断努力,以实现这样的梦想。
“我们谈论的是让年老或生病的人重新焕发活力,让他们的整个身体或特定器官重新焕发青春,从而让疾病消失,”他说。“这是个好主意。这不是我们通常做药的方式。”
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
【首都师范大学是211吗】一、“首都师范大学是211吗”是许多考生和家长在选择大学时经常提出的问题。实际上,...浏览全文>>
-
【首都师范大学科德学院自考和统招毕业证不一样吗有什么不一样的】在选择继续教育方式时,很多学生都会关注“...浏览全文>>
-
【首都师范大学科德学院自考本科国家承认学历吗】一、“首都师范大学科德学院自考本科国家承认学历吗”是许多...浏览全文>>
-
【首都师范大学科德学院怎么样首都师范大学科德学院介绍】首都师范大学科德学院是一所位于北京市的全日制本科...浏览全文>>
-
【第一次电影剧情】《第一次》是一部由美国导演理查德·林克莱特(Richard Linklater)执导的电影,于2004年...浏览全文>>
-
【首都师范大学科德学院学费一年多少钱】首都师范大学科德学院是一所经教育部批准设立的全日制本科独立学院,...浏览全文>>
-
【第一次点外卖的流程】对于第一次尝试点外卖的人来说,整个过程可能会有些陌生。不过,只要按照步骤来,就能...浏览全文>>
-
【首都师范大学科德学院学费为什么要这么贵】首都师范大学科德学院作为一所独立学院,近年来在学费方面引发了...浏览全文>>
-
【第一次登泰山的忌讳】泰山,作为五岳之首,不仅是中国文化的重要象征,也是无数人心中的朝圣之地。对于第一...浏览全文>>
-
【首都师范大学科德学院位于哪个城市】首都师范大学科德学院是一所独立学院,隶属于首都师范大学。对于许多学...浏览全文>>
