DNA修复方案更接近癌症治疗
来自莱斯大学和田纳西州孟菲斯市圣裘德儿童研究医院的研究人员仔细研究了细胞修复断裂 DNA 链的一种方式,并发现了有助于使特定酶成为精准癌症治疗有希望的靶点的细节。
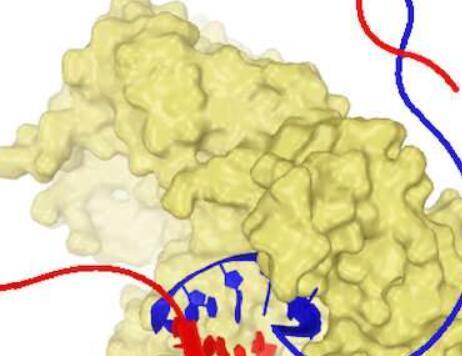
与修补轮胎不同,DNA 聚合酶 theta(又名 Pol theta)的工作是修复DNA 中的双链断裂,桥接悬挂的单链末端并催化断裂处的 DNA 合成,这一过程称为微同源介导的末端加入(MMEJ)。
MMEJ 与其他两个修复 DNA 双链断裂的过程——同源重组和非同源末端连接——互补,但保真度较低,因为 Pol theta 容易发生突变、插入和删除错误。
但其中存在优势:MMEJ 需要 Pol theta 来修复双链。
Rice 和 St. Jude 的研究人员在《核酸研究》杂志上进行的一项新研究首次揭示了 Pol theta 介导的 MMEJ 的结构基础,展示了其独特的插入环如何在为 MMEJ 修复准备位点时帮助稳定短 DNA 结合.
莱斯大学生物科学助理教授高洋、圣裘德大学结构生物学系助理教授孙继以及博士后研究员李楚轩和圣裘德大学的朱汉文领导了这项研究。
“当 DNA 断裂时,对细胞来说是非常危险的,细胞必须立即修复它,”德克萨斯州癌症预防与研究所 (CPRIT) 研究 DNA 复制机制的癌症研究学者高说。“一次休息就可以细胞,细胞不想死,尤其是癌细胞。
“最常见的情况之一是患者有 BRCA1 或 BRCA 2 突变,”他说。当健康时,这些基因会表达 DNA 修复蛋白,但突变会引发乳腺癌。“当患者的这些基因出现问题时,他们无法通过同源重组途径进行修复。他们必须走其他途径。
“八年前人们发现,当他们敲除正常细胞中的 Pol theta 时,它不会成为问题,”高说。“但如果这种蛋白质的敲除发生在具有突变 BRCA1 或 BRCA2 的细胞中,这些缺陷可能是致命的。这就是使它成为一个非常有前途的药物靶点的原因。Pol theta 抑制剂不会伤害正常细胞,只会伤害癌细胞。”
他说,基于其他实验室的研究,此类治疗的临床试验正在进行中,但赖斯实验室的研究增加了有关该机制的细节。
李指出,虽然新论文中的实验是针对从亚洲海鲈鱼中提取的蛋白质,但她的工作仍在人类版本上继续进行。
“我喜欢这个项目,”她说。“我认为可以专门针对这种酶做很多事情,因为它是如此独特。我相信会有更多人有动力研究这种特殊的蛋白质。”
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
【首都师范大学是211吗】一、“首都师范大学是211吗”是许多考生和家长在选择大学时经常提出的问题。实际上,...浏览全文>>
-
【首都师范大学科德学院自考和统招毕业证不一样吗有什么不一样的】在选择继续教育方式时,很多学生都会关注“...浏览全文>>
-
【首都师范大学科德学院自考本科国家承认学历吗】一、“首都师范大学科德学院自考本科国家承认学历吗”是许多...浏览全文>>
-
【首都师范大学科德学院怎么样首都师范大学科德学院介绍】首都师范大学科德学院是一所位于北京市的全日制本科...浏览全文>>
-
【第一次电影剧情】《第一次》是一部由美国导演理查德·林克莱特(Richard Linklater)执导的电影,于2004年...浏览全文>>
-
【首都师范大学科德学院学费一年多少钱】首都师范大学科德学院是一所经教育部批准设立的全日制本科独立学院,...浏览全文>>
-
【第一次点外卖的流程】对于第一次尝试点外卖的人来说,整个过程可能会有些陌生。不过,只要按照步骤来,就能...浏览全文>>
-
【首都师范大学科德学院学费为什么要这么贵】首都师范大学科德学院作为一所独立学院,近年来在学费方面引发了...浏览全文>>
-
【第一次登泰山的忌讳】泰山,作为五岳之首,不仅是中国文化的重要象征,也是无数人心中的朝圣之地。对于第一...浏览全文>>
-
【首都师范大学科德学院位于哪个城市】首都师范大学科德学院是一所独立学院,隶属于首都师范大学。对于许多学...浏览全文>>
